又有1款醫(yī)療器械獲特別審批 8款將進(jìn)優(yōu)先審批
??? 4月21日�,CFDA發(fā)布公示信息��,共有1款醫(yī)療器械將獲特別審批�,8款將進(jìn)入優(yōu)先審批。
? 一款醫(yī)療器械進(jìn)入優(yōu)先審批
? 4月21日���,CFDA醫(yī)療器械技術(shù)審評(píng)中心發(fā)布《醫(yī)療器械優(yōu)先審批申請(qǐng)審核結(jié)果公示(2017年第3號(hào))》�,如果不出現(xiàn)意外��,又一款國(guó)產(chǎn)醫(yī)療器械即將獲國(guó)家優(yōu)先審批����。
? 據(jù)公示信息,該產(chǎn)品名稱(chēng)為“藥物洗脫球囊導(dǎo)管”���,申請(qǐng)人為遼寧垠藝生物科技股份有限公司����。申請(qǐng)中心認(rèn)為����,該產(chǎn)品為“臨床急需、且在我國(guó)尚無(wú)同品種產(chǎn)品獲準(zhǔn)注冊(cè)的醫(yī)療器械����;可用于冠脈分叉病變”��。
? 賽柏藍(lán)器械查詢(xún)CFDA相關(guān)數(shù)據(jù)�����,同類(lèi)進(jìn)口產(chǎn)品沒(méi)有檢索到�,國(guó)內(nèi)名稱(chēng)完全相同的產(chǎn)品也沒(méi)有檢索到���。
? 但有一款名稱(chēng)相似的國(guó)產(chǎn)器械在去年5月25日獲批�����。該產(chǎn)品是由北京先瑞達(dá)醫(yī)療科技有限公司注冊(cè),其名稱(chēng)為“藥物洗脫外周球囊擴(kuò)張導(dǎo)管”�����,CFDA要求該產(chǎn)品在注冊(cè)獲批后�,還要完成以下工作:在產(chǎn)品上市后開(kāi)展以12個(gè)月靶血管通暢率為主要觀(guān)察終點(diǎn)的注冊(cè)研究,隨訪(fǎng)至少1年��,在延續(xù)注冊(cè)時(shí)提交統(tǒng)計(jì)分析報(bào)告�����。
? 據(jù)了解,遼寧垠藝生物成立于2004年����,是完全由高校科技人員創(chuàng)辦的企業(yè)��,主要從事心血管支架等三類(lèi)介入醫(yī)療器械研發(fā)���、生產(chǎn)和銷(xiāo)售�����。
? 據(jù)悉���,這是今年以來(lái)CFDA優(yōu)先審批的第3款醫(yī)療器械產(chǎn)品。前兩款產(chǎn)品都已經(jīng)列入國(guó)家重點(diǎn)研發(fā)計(jì)劃���,分別是成都?xì)W賽醫(yī)療器械有限公司申請(qǐng)的“中空纖維膜血液透析濾過(guò)器”�����,廣州市暨華醫(yī)療器械有限公司申請(qǐng)的“血液透析/濾過(guò)裝置”�����。
? 8款創(chuàng)新醫(yī)療器械進(jìn)入特別審批
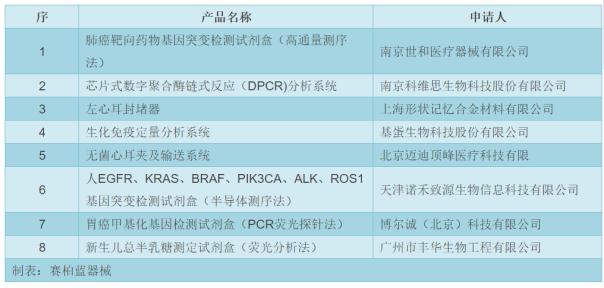
? 同一天�����,該中心還發(fā)布了《創(chuàng)新醫(yī)療器械特別審批申請(qǐng)審查結(jié)果公示(2017年第3號(hào))》�,又有8款創(chuàng)新醫(yī)療器械進(jìn)入特別審批通道,如無(wú)異議����,即將生效。這8款產(chǎn)品及申請(qǐng)企業(yè)情況如下:
?